第七例艾滋病缓解病例为更多人带来长期治疗的希望
发布日期:2025-12-15 12:47 点击次数:89

在抗击人类免疫缺陷病毒(HIV)的漫长战役中,医学界长期以来一直将目光锁定在一种罕见的基因突变上。这种被称为CCR5-Δ32的“黄金突变”,被认为是开启治愈大门的唯一钥匙。然而,本周《自然》杂志披露的一项重磅研究成果,正在重新改写这一教科书般的认知。
来自德国柏林夏里特医学院的研究团队确认,一名被代称为“第二位柏林病人”(Berlin Patient 2,简称B2)的男子,在接受异体造血干细胞移植六年后,体内的HIV病毒载量持续检测不到,临床上已被认定为“长期缓解”甚至可能已经治愈。
这一案例的轰动之处不在于“治愈”本身——毕竟此前已有数例类似先例——而在于他打破了以往成功的必要条件:他的干细胞捐赠者并非携带双拷贝突变的“完美匹配者”,而仅仅携带了一个保护性基因拷贝。这一发现不仅撼动了现有的治疗理论基石,更为全球数千万无法找到完美供体的HIV感染者点亮了新的希望灯塔。
走出“双突变”迷思:B2病例的医学突破
(SciePro/Science Photo Library/Getty Images)
长期以来,著名的“柏林病人”(第一位)蒂莫西·雷·布朗的成功案例确立了干细胞移植治愈艾滋病的标准范式。布朗接受了携带纯合子CCR5-Δ32突变(即双拷贝突变)的干细胞移植。这种突变导致免疫细胞表面缺乏CCR5受体——这是HIV病毒入侵人体细胞的主要“门户”。由于病毒找不到进入细胞的把手,感染链条被物理切断,从而实现治愈。
然而,寻找双拷贝突变的供体如同大海捞针。这种基因型主要存在于北欧人群中,且仅占总人口的约1%。对于绝大多数需要移植的HIV合并白血病患者而言,找到配型相合且携带双拷贝突变的供体概率微乎其微。
B2病例的出现打破了这一僵局。这位患者于2009年确诊感染HIV,2015年又不幸罹患急性髓系白血病,生命垂危。在筛选供体时,医生未能找到携带双拷贝突变的完美人选,最终选择了一位携带杂合子突变(即单拷贝突变)的供体。理论上,单拷贝突变只能减少细胞表面的CCR5受体数量,而不能完全消除它们,因此过去认为这不足以完全阻断病毒复制。
令人惊讶的是,在接受移植并于2018年停止抗逆转录病毒治疗(ART)后,B2并未出现病毒反弹。截至目前,经过长达六年的严密监测,其血液和组织样本中均未检测到具有复制能力的病毒库残留。这一结果向科学界提出了一个尖锐的问题:如果不再需要完美的“防盗门”,那么究竟是什么清除了体内的病毒?
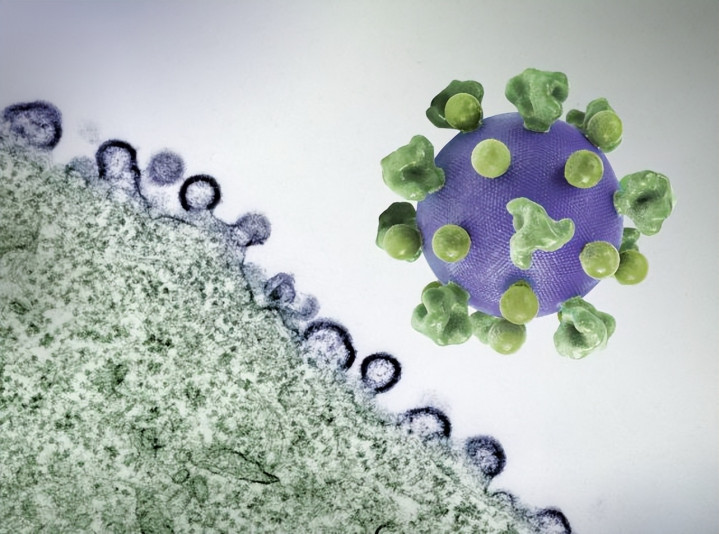
图中右侧为HIV病毒颗粒的3D打印模型,旁边是受感染细胞的彩色显微照片。(图片来源: NIAID/Wikimedia Commons)
免疫重塑与病毒库清洗:深层机制的再审视
夏里特医学院免疫学家、该研究的主要作者克里斯蒂安·盖布勒博士指出,B2的成功可能揭示了“移植物抗病毒效应”(Graft-versus-Viral-Reservoir Effect)在治愈过程中的核心作用。
在干细胞移植过程中,患者原有的免疫系统首先通过大剂量化疗被彻底摧毁。这一过程不仅杀死了癌细胞,也清除了绝大部分潜伏着HIV病毒的免疫细胞。随后,来自供体的新免疫系统接管了身体。这些新细胞会将患者体内残留的旧细胞识别为“外来物”并进行攻击。这种免疫攻击在癌症治疗中被称为“移植物抗白血病效应”,而在HIV治疗中,它可能扮演了“清道夫”的角色,系统性地搜寻并消灭了所有潜伏病毒的残余堡垒。
此外,虽然单拷贝突变不能完全关闭CCR5受体的大门,但它确实降低了病毒入侵的效率。研究人员推测,当病毒入侵变得困难(虽然不是不可能),同时又面临新免疫系统的猛烈围剿时,病毒的复制能力最终耗尽,从而导致了病毒库的彻底枯竭。
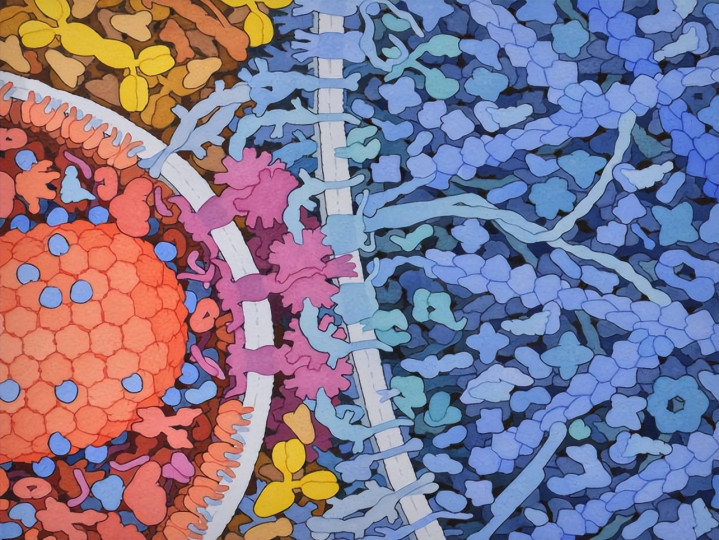
图示:艾滋病毒(左)附着于细胞。(David S. Goodsell,斯克里普斯研究所)
这一假说也得到了“日内瓦病人”案例的支持。日内瓦病人接受了完全不携带任何CCR5突变的普通干细胞移植,却依然实现了长期缓解。相反,此前波士顿的两例类似患者却经历了病毒反弹。这种差异表明,除了基因突变,移植后的免疫反应强度、化疗方案的彻底性以及个体差异等复杂因素共同决定了最终的成败。B2病例证明,极度的病毒库缩减,配合一定程度的受体保护,可能足以跨越“治愈”的门槛。
从个案到普惠:未来治疗策略的转型
尽管干细胞移植疗效显著,但医学专家反复强调,这种高风险疗法绝不可能成为HIV的常规治疗手段。移植手术伴随着高达10%至20%的死亡率,且受者需要终身服用免疫抑制剂,这种代价对于仅仅感染HIV但可以通过药物控制病情的普通患者来说是不可接受的。
然而,B2病例的价值在于它为基因编辑和免疫疗法指明了新方向。既然单拷贝突变就能奏效,那么未来的基因编辑疗法(如CRISPR技术)可能不需要追求100%的基因敲除效率。只要能将患者体内一部分细胞的CCR5基因进行修改,或者通过药物模拟单拷贝突变的效果,再配合增强免疫系统识别病毒库的能力,或许就能达到“功能性治愈”的目标。
目前,全球已有七例公认的艾滋病缓解或治愈病例。从最初的偶然奇迹,到如今对机制的深入解析,人类对抗这一世纪顽疾的战线正在稳步推进。B2的故事告诉我们,治愈艾滋病的道路或许比我们预想的要宽广——它不再仅仅依赖于寻找那个百万分之一的完美供体,而是可以通过多维度的免疫调节和病毒库清除策略来实现。
正如国际艾滋病协会主席所言,虽然我们距离普及性的解药还有很长的路要走,但每一个像B2这样的“幸存者”,都在为最终终结艾滋病大流行拼凑出至关重要的一块拼图。对于全球3900万HIV感染者而言,科学界正在逐步解开病毒潜伏的最后一道枷锁,让“治愈”从一个遥不可及的医学神话,逐渐转变为可复制的临床现实。